都市域から排出された疎水性の汚染物質(hydrophobic pollutants)は、そのまま海に流れ出さずに、汽水域の底質に蓄積していきます。Murphyら(1988;下の論文からの孫引き)によると、90%以上の懸濁態炭化水素が汽水域にとどまる場合があるそうです。
では、なぜそのようなことが起こるのか?なぜ汽水域で疎水性物質が蓄積するのか?そのメカニズムを、塩分とDOM(Dissolved Organic Matter)に着目して調査したのが下の論文です。以前、底質へのPAHs吸着と塩分・粒子径の関係を調べた論文を紹介しましたが、その元ネタ的な論文です。これが中々勉強になりました。
Brunk B.K. et al., 1996, Effects of salinity changes and the formation of dissolved organic matter coatings on the sorption of phenanthrene: Implications for pollutant trapping in estuaries, Environ. Sci. Technol., 31 (1), 119-125.
PAHの懸濁物質(カオリンなど)への吸着・収着は、塩分と共存するDOMの種類を変更した時にどう変化するのかを調べています。その結果から、汽水底質にPAHなどの疎水性物質が蓄積する理由を説明できるか、平衡分配モデルで検証しています。

図:上記論文より作成
■塩分と平衡分配の関係
まず本論文の上の図を参考に「PAHの収着の平衡に塩分がどう作用するのか」を理論的に整理したいと思います*1。DOMはとりあえず無視します。
ここで考える対象物質は
だけです。
まず、「PAHのSSへの収着が平衡状態にあるのは、どういう時か」を考えます。収着が平衡状態に達しているとすると、
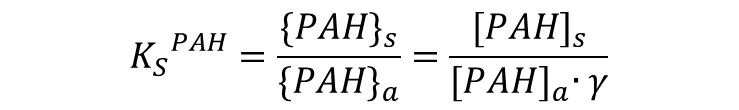 式1
式1という式が成り立ちます(式1)。ここで{PAH}aは溶存態のフリーPAHの活量で、{PAH}sはSSに収着しているPAHの活量です。K s,PAHはSSと液中の分配係数(distribution coefficient)で、温度や塩分が一定ならばK s,PAHはある一定の値に達します。式から、K s,PAHが大きい系はSSに収着しやすい系を意味することが分かります。また「濃度×活量係数γ=活量」という関係が成り立つので、最右辺のように式を変形できます。SS収着態における活量と濃度の関係がよく分からないのですが、どうやら「活量=濃度(g/g-SS)」とみなしても良さそうなので*3、上式のようになります。溶存態では、希釈溶液で活量係数γが1とみなせる時は、「活量=濃度」となります。
次に、「塩分の変化が溶存態のPAHにどう影響するのか」を考えます。
上に書いたように溶存態においては 、「濃度×活量係数γ=活量」という関係が成り立ちます。そしてPAHのような非電解質の活量係数γは、イオン強度Iと下のような関係にあります(式2)。
 式2
式2
Iはイオン強度(mol/L)、ksは塩析係数(salting coefficient)(L/mol)です。この式は非電解質の活量係数に関する経験式で、ksは実験的に求められます。(ちなみに電解質の場合、イオン強度と活量係数の間にはデバイ-ヒュッケルの式が成り立ちます。非電解質と電解質のどちらを対象とするかで、活量係数とイオン強度との関係は、傾向が反対になります。詳細はSnoeyink and Jenkins, Water Chemistry, Wiley, p.80, 1980.)
この式を見れば、塩分が増加すると(=イオン強度が増加すると)、非電解質(ここではPAH)の活量係数が増加することが分かります。活量係数が増加すれば、「濃度×活量係数γ=活量」ですから、活量も増加します。
話をまとめると、非電解質が同濃度の場合「海水では純水に比べて非電解質の活量が大きくなる」ということになります。イメージとしては次のように捉えると分かりやすいでしょう。海水では塩類イオンが水分子を強く引きつけ、水和水として固定します。そのため非電解質が溶けられる水分子の量は減少し、実質的な濃度、つまり活量は増加するわけです。
最後に、上の2つの式をまとめて「PAHの収着の平衡に塩分がどう作用するのか」を考えます。式1の{PAH}s/{PAH}aは純水でも、海水でも一定なので、式1と式2をまとめて、
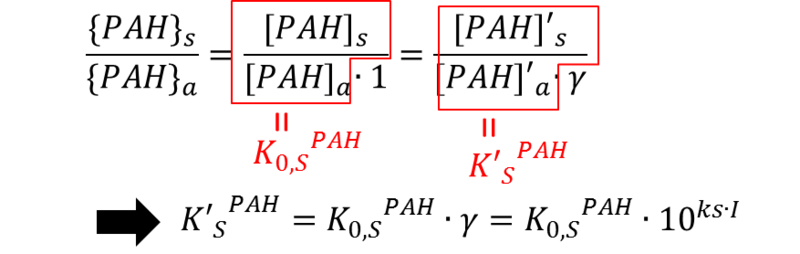
となります。K 0,s,PAHは純水中の分配係数で、K’ s,PAHは海水中の平衡定数です。最後の式を見ると、イオン強度Iが増加する、すなわち塩分が増加するとK’ s,PAHが増加することが分かります。つまり、「塩分が高いほどPAHのような非電解質はSSに吸着しやすくなる」というわけです。
■DOMと平衡分配の関係
今度は本論文のもう一つの軸であるDOMと収着の関係を整理します。こちらは割とイメージしやすい話です。ざっくり結論を書くと、上の図に描かれているようにDOMの共存下でPAHはDOMに収着し、そのDOMがSSにくっつくため、結果としてSSへのPAH収着量は増加します。
この関係を式で書いてみましょう。ここでは、塩分の話は一旦脇においておきます。なので、活量ではなく全て濃度で考えましょう。SS,PAHにDOMを加えた系での固液相全体での分配係数をK0とすると、
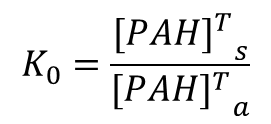
のように表せます。ここで、[PAH]T,sは「固相への合計収着濃度(g/g-SS)」を示し、[PAH]T,aは「液相における合計濃度(g/mL)」を示します。そして、[PAH]T,sと[PAH]T,aはその定義から、次のように表せます。
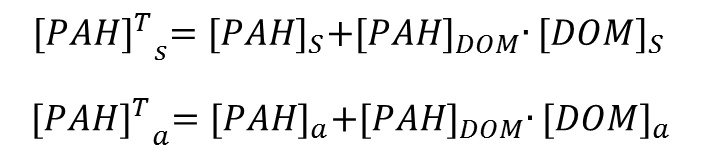
ここで[PAH]s, [PAH]aはそれぞれSS吸着PAH濃度(g/g-SS)、溶存態フリーPAH濃度(g/mL)を表します。[PAH]DOMはDOM収着PAH濃度(g\g-DOM)を、[DOM]sと[DOM]aはそれぞれSS吸着DOM濃度(g-DOM/g-SS)、溶存態DOM濃度(g-DOM/mL)を表しています。
この関係を上のK0の式に代入して整理すると、
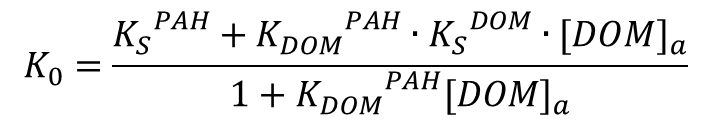
という式が導かれます。個々の分配係数の定義はその記号(添え字)の通りなので省略しますが、溶存態DOM濃度と分配係数が得られれば、全体の分配係数K0が求められることが上式より分かります。
■汽水域でのトラップは平衡分配で説明できない?
本論文では、上記理論と実験結果を併せ、SS,PAH,DOMの存在する系での固液相全体での分配係数K0と塩分との関係を求めました。そしてその結果を実際の汽水域底質で観測されたデータと比較しました。
すると、実際の汽水域環境において固相に存在するPAH割合は、この論文の平衡分配計算・実験で想定された割合よりも、数100倍も高かったのです。つまり、汽水域でPAH(のような疎水性物質)が固相に捕捉されるという現象に対して平衡分配が果たす寄与は極めて少ないと推測されます。
やはり実環境の濃度を考える時には、隔離(sequestration)のような現象が重要なのでしょう。

Water Chemistry (Spe Monographs)
- 作者: Vernon L. Snoeyink,David Jenkins
- 出版社/メーカー: John Wiley & Sons
- 発売日: 1980/04/17
- メディア: ハードカバー
- この商品を含むブログを見る